近日,武汉科技大学医学部田波团队与华中科技大学同济医学院张培团队在PNAS杂志在线发表了题为“Divergent BLA engram circuits orchestrate social preference dynamics in bystander male mice with self-experienced stress”的研究论文。该研究建立了一种联合单次社交失败应激(single social defeat stress,SSDS)和替代性社交失败应激(vicarious social defeat stress,VSDS)的小鼠模型,结合光遗传学、光/化学遗传学、病毒示踪、在体电生理记录等技术,阐明了源自BLA记忆印迹细胞的多级输出环路在社交偏好和社交回避行为调控中的神经机制。
个体自身经历对其社交选择的灵活性具有重要调控作用,该现象背后蕴含着趋利避害的生物进化本质。社交灵活性不仅是个体塑造健康心理状态、实现心理适应的重要过程,更是社会关系得以建立、发展与维持的核心环节。以往研究已证实,个体先前的社交相关自身经历,会对社交认知、社交偏好及社交回避等各类社会行为产生重大影响。然而,先前社交经历的相关信息如何转化为后期适应性社交行为的神经机制尚不清楚。
大量研究表明,基底外侧杏仁核(basolateral amygdala,BLA)在社交失败应激相关创伤记忆的储存、再巩固和提取中发挥重要的作用。课题组前期也证实了社交失败创伤记忆由BLA印迹细胞(BLA engram cells,BLAEC)存储与编码(Neuron,2024)。“记忆印记细胞”(Engram cells)的科学概念最早由Richard Semon于1904年提出,将机体事件经历在神经系统中留下的持久物理与化学改变命名为记忆印迹(Engram),认为特定神经元群被经验激活并发生可塑性修饰后,可在后续线索触发下重新激活以实现记忆提取。因此,作者推测BLA记忆印记细胞可能参与驱动具有社交失败经历个体的后续社交灵活性,包括社交偏好和社交回避行为。

研究人员首先检测了替代性社交失败应激(vicarious social defeat stress, VSDS)处理下小鼠社交的基线水平,发现VSDS组与对照组无显著差异:实验对象偏好与新小鼠社交而非有类似创伤经历的同伴,同时并不对攻击性CD1鼠产生社交回避(图1)。
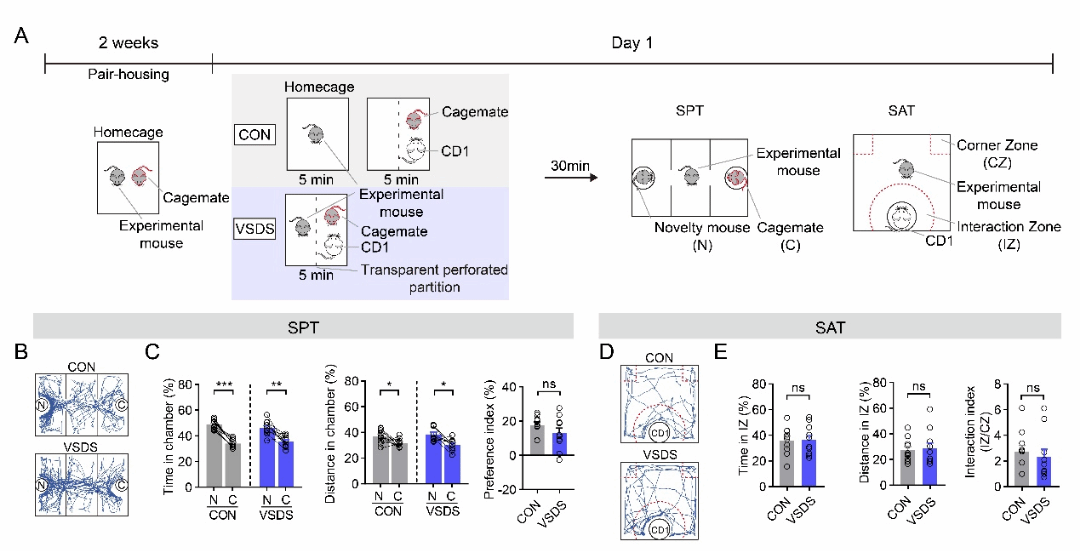
图1.早期的创伤性自我经历会影响小鼠的社交偏好动态
随后检测单次社交失败应激(single social defeat stress,SSDS)对小鼠社交的影响,结果发现SSDS组小鼠偏好与有类似创伤经历的同伴社交,同时对攻击性CD1鼠产生社交回避。有趣的是,这种社交改变维持约两周后消失,并且可被VSDS再次诱发(图2)。
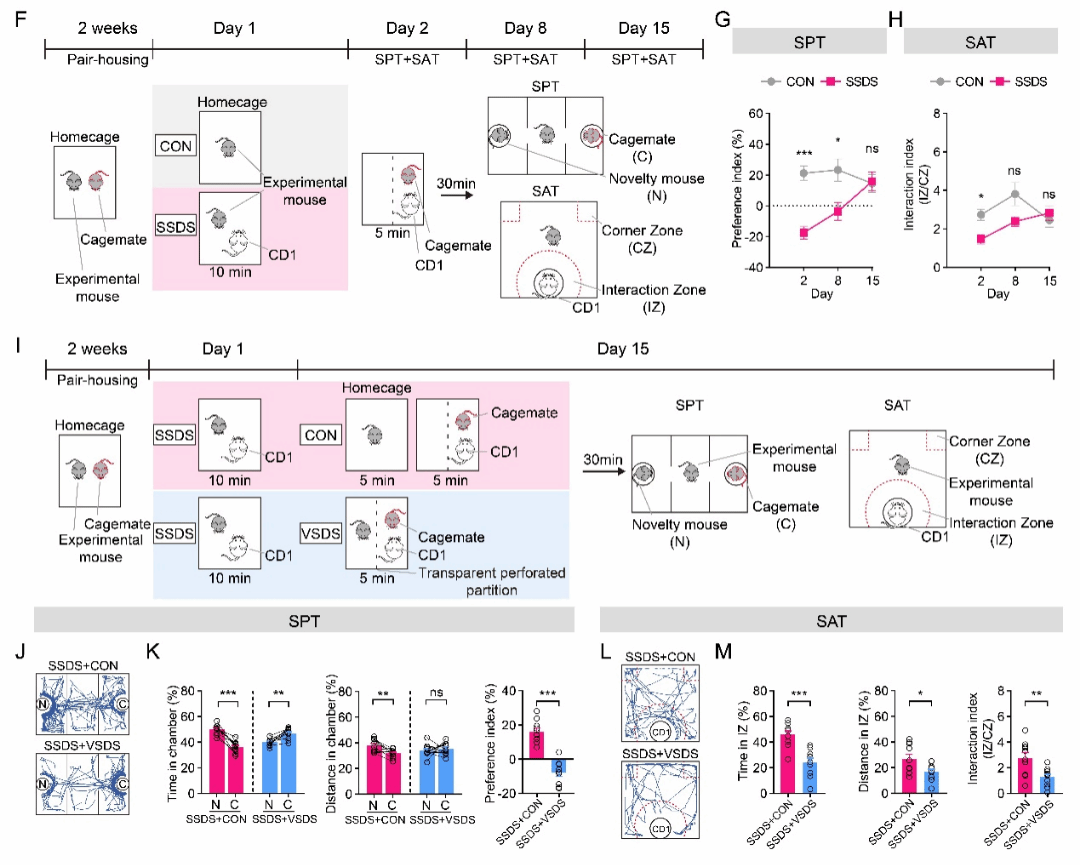
图2. SSDS相关BLA印迹细胞会对处于劣势的同笼伙伴或攻击者的社交活动产生响应
通过BLA印迹细胞标记技术与光纤钙成像技术,发现BLA中与SSDS相关的印迹细胞在小鼠与有类似创伤经历的小鼠和CD1鼠社交时活性显著增加(图3)。化学遗传学调控证实了BLAEC在社交偏好行为动态改变中的充分性和必要性。
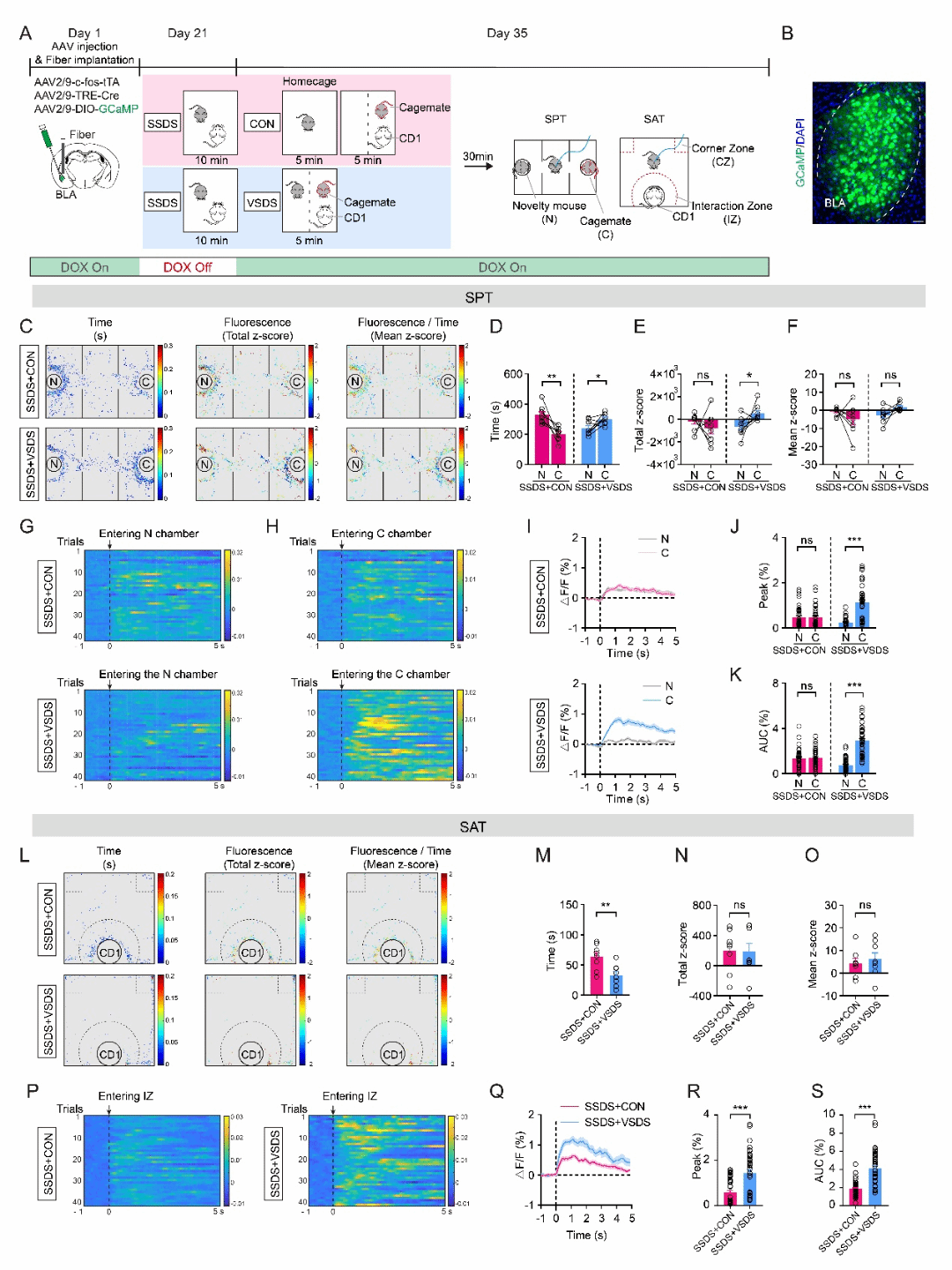
图3.双向化学遗传学操控BLA印迹细胞能够模拟或阻断VSDS小鼠的SSDS经历的社会偏好动态
为进一步探究其神经环路机制,研究团队通过病毒示踪技术与光纤记录技术,证实BLAEC-ACCGLU环路的结构连接和功能连接(图4)。
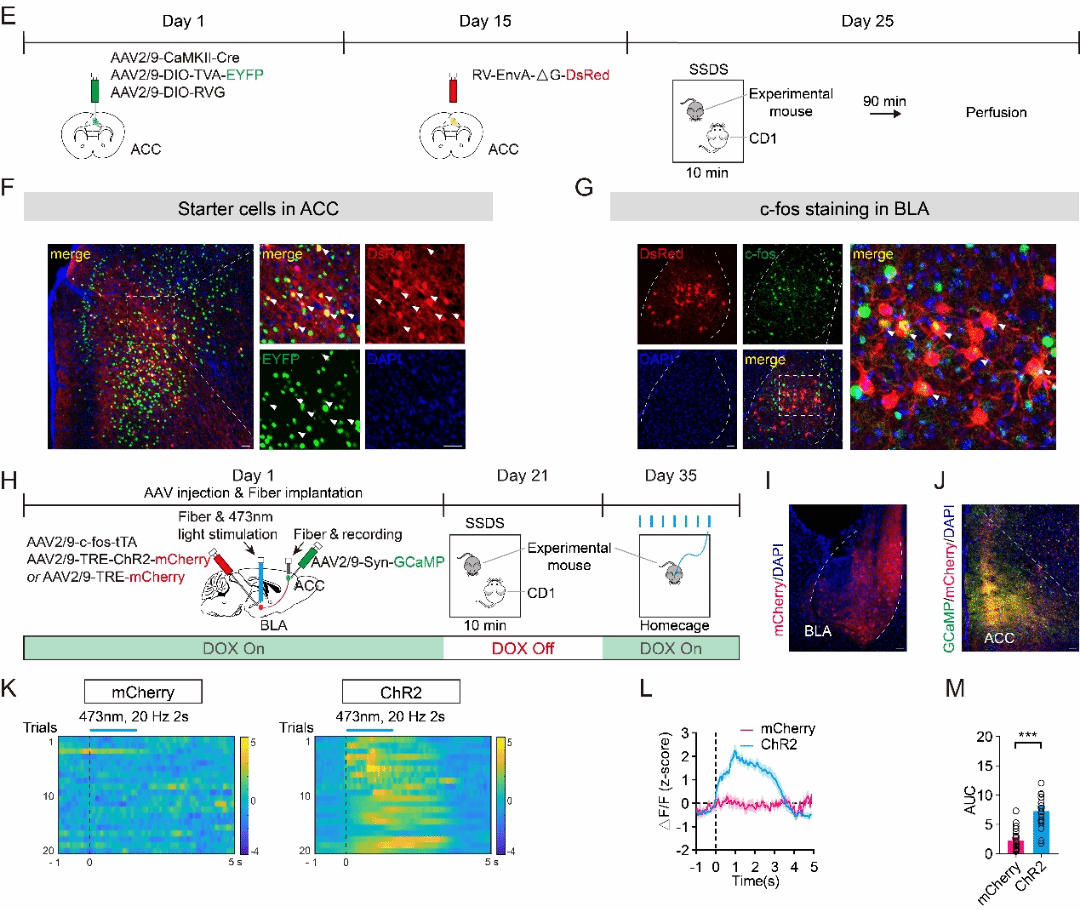
图4. 基于病毒示踪技术的全脑映射实验揭示了BLAEC会投射至ACCGlu神经元
通过光遗传手段双向调控该环路,研究人员发现激活BLAEC-ACC环路可以模拟VSDS的作用;抑制BLAEC-ACC环路可以阻断VSDS对SSDS经历小鼠的社交偏好和社交回避的作用(图5)。
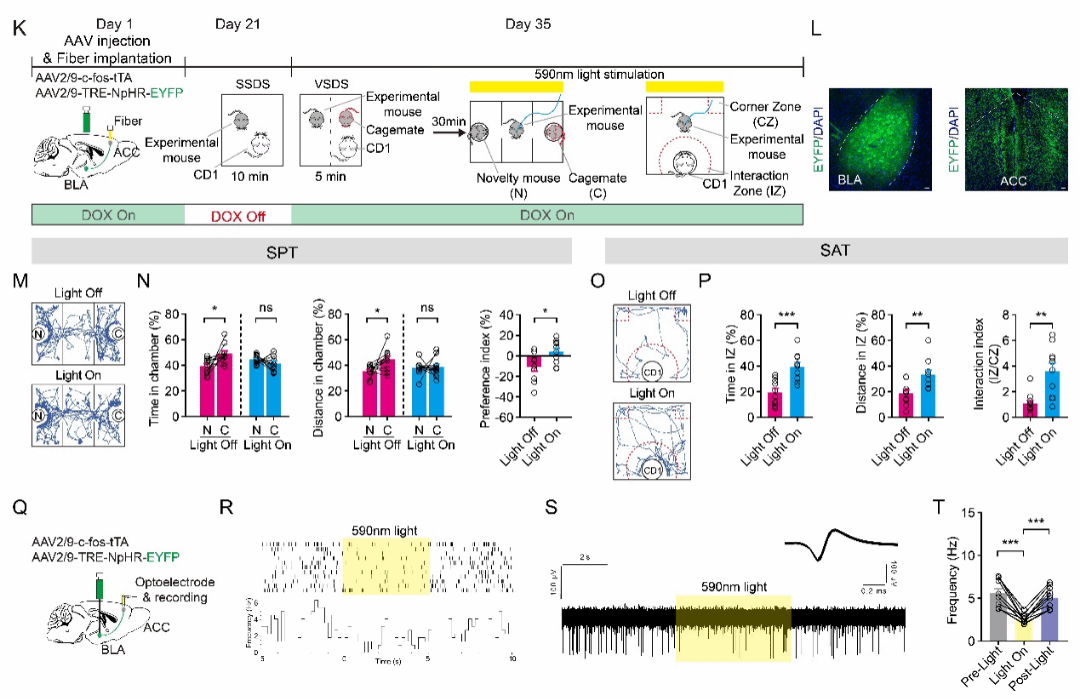
图5. BLAEC-ACC环路调控经历过SSDS的VSDS小鼠的社交偏好动态
进一步实验发现,BLA-ACC环路的下游投射dHPC/vHPC/ZI对不同维度的社交行为产生影响:BLA-ACC-dHPC环路调节社交偏好行为,BLA-ACC-vHPC环路调节社交回避行为,BLA-ACC-ZI环路调节社交偏好行为和社交回避行为(图6)。
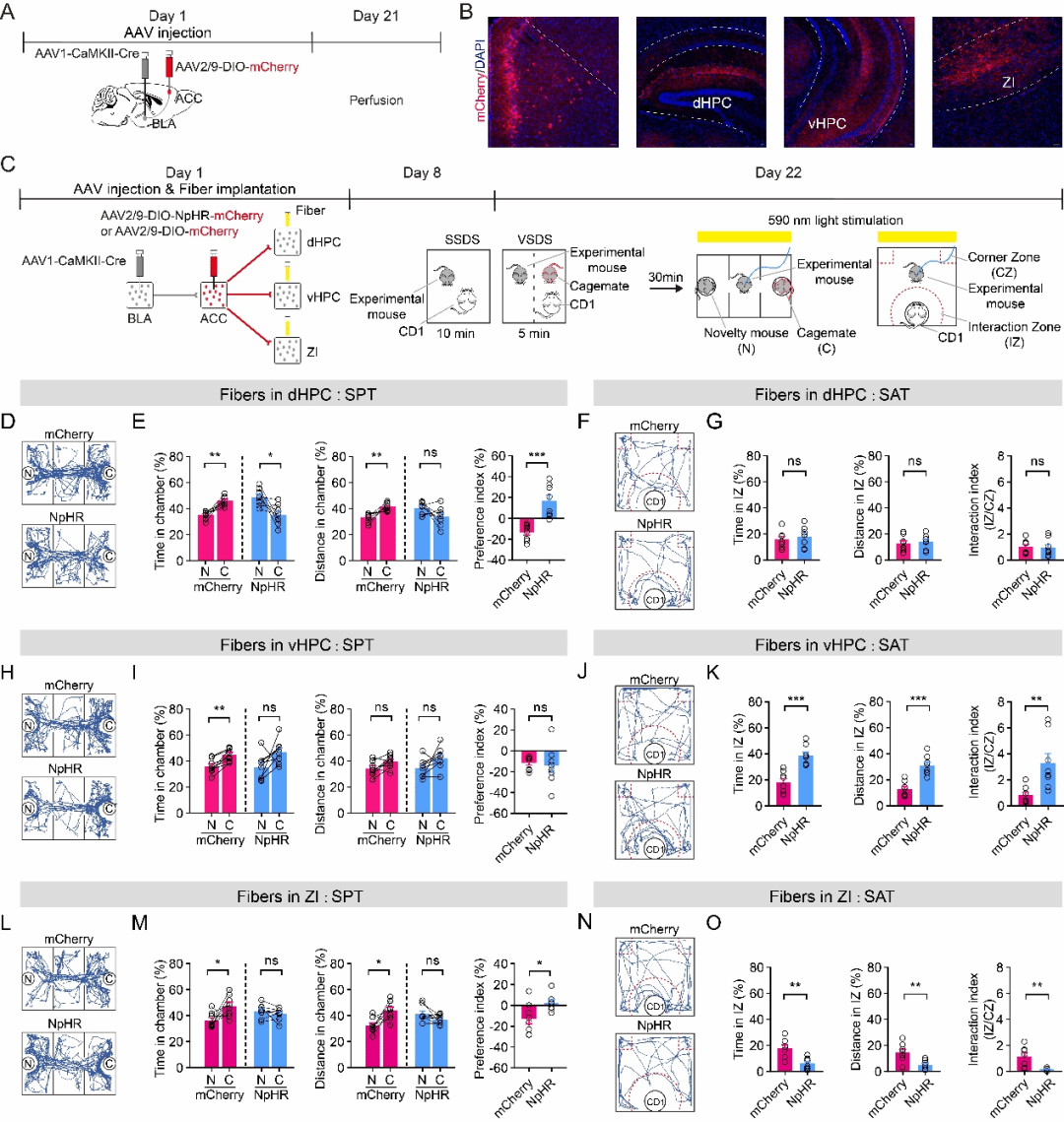
图6. BLA-ACC环路的不同投射对经历过SSDS的VSDS小鼠的社交偏好动态产生了不同的影响
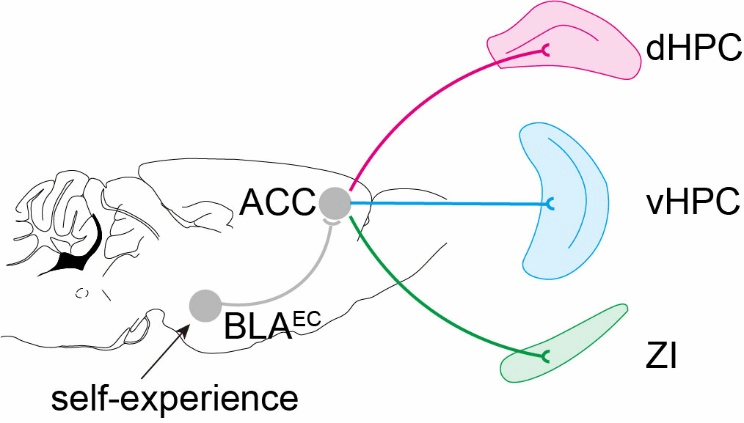
本研究解析了源自BLA记忆印记细胞的下游多级环路BLA-ACC-vHPC、BLA-ACC-dHPC、BLA-ACC-ZI分别调控不同维度的社交行为。
本研究存在以下局限性:其一,样本仅局限于雄性小鼠,结论的群体推广性受限。后续研究有必要在雌性小鼠中验证相关发现,以提供更全面的解释。其二,接受上游BLA记忆印记细胞投射的ACC神经元群体,向下游海马与未定带投射在空间分布上是否存在差异性,这些空间分布结构差异是否与社交偏好功能维度相重合,仍有待进一步解析。
综上,本研究从“记忆印记细胞”的角度,明确了早期社交失败经历驱动社交行为灵活性的环路机制,进一步加深了我们对社交行为与社交障碍相关脑疾病发生机制的理解。
课题组简介:课题组致力于联合应用分子生物学、细胞生物学、动物行为学、病毒神经示踪、光/化学遗传学、在体电生理、在体钙成像、转录组学、蛋白组学、生物信息学等相关技术,解析多巴胺能神经元参与生理(如共情、恐惧记忆的形成和消退)和病理(如帕金森病、抑郁症、PTSD)过程的神经环路机制及分子机制。课题组长田波教授在中外期刊上发表论文80余篇,其中以通讯作者或第一作者在包括Neuron、Nature Cell Biology、PNAS、Nature Communications、Gastroenterology、PLOS Biology、Neuropsycopharmacology、Cell Reports等高水平期刊发表论文。以第一申请人申请和获批国家发明专利和实用新型专利6项。近年来主持国家自然科学基金项目6项,主持多项省部级及企业横向项目,获湖北省杰青项目。